uv reactors, photo-oxidation, advanced oxidation (aop), recycling & engineering
for industrial use
UV-Oxidation
Foto-Oxidation
Chemie der UV-Oxidation und von UV Advanced Oxidation
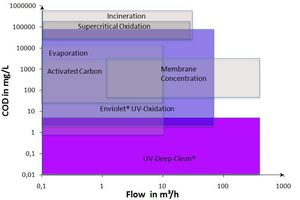
Chemie der UV-Oxidation und von UV-basierten Advanced Oxidation Prozessen
Enviolet ist der Spezialist im Bereich der UV-AOP (Advanced Oxidation Process) bei industriellen Anwendungen. Dabei verfügen wir über zwei unterschiedliche Prozessfamilien: auf der Basis der Foto-Oxidation und der UV-Oxidation (UV Advanced Oxidation).
- Enviolet®: die UV-Oxidation / Advanced Oxidation im Bereich höher Konzentrationen in der homogenen Phase
- UV deep clean: die UV-Oxidation in der heterogenen Phase zum Erreichen geringster Endkonzentrationen (Foto-Oxidation).
Grundlagen der UV-Oxidation
Die Voraussetzung einer Fotoreaktion (UV-Oxidation) eines Moleküls R ist die Absorption von Licht durch dieses Molekül (Calvert und Pitts, 1966). Der Betrag dieses absorbierten Lichtes A(λ) wird durch das Lambert-Beer’sche Gesetz beschrieben, wobei I(0) die Lichtintensität vor der Lösung und I die Lichtintensität nach dem Durchgang durch die Lösung ist. Linear abhängig ist die Absorption von der Konzentration C der Schichtdicke d und dem dekadischen Extinktionskoeffizienten ε(λ).
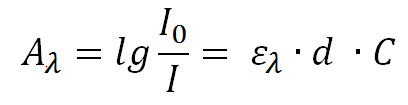
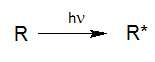
Bei der Absorption von Licht mit ausreichender Energie entsteht aus dem Molekül R ein energiereicheres, angeregtes Molekül R*, dessen Energiegehalt um die zugeführte Photonenenergie erhöht ist. Grundsätzlich ist diese Absorption die notwendige Vorrausetzung für jede Art von Fotoreaktion (UV-Oxidation). Diese bedeutet, zunächst, dass auch sehr dunkle oder stark gefärbte Lösungen gut für eine UV-Oxidation geeignet sind, wenn die Bauweise der UV-Reaktoren dafür geeignet ist.
R* kann aus diesem Zustand in einer UV-Oxidation direkt oder über reaktive Intermediäre in den Grundzustand zurückgehen oder physikalisch zu Fotoprodukten weiterreagieren. Durch sich anschließende chemische Prozesse entstehen in wässrigen Lösungen Radikale, Radikalionen, Ionen oder stabile Fragmente, welche durch thermische Prozesse weiterreagieren können.
In der Gegenwart von Oxidationsmitteln kommen weitere Reaktionswege hinzu:
So kann z.B. Wasserstoffperoxid (H2O2) durch Licht geeigneter Wellenlänge in hochreaktive Hydroxylradikale photolysiert werden, die mit organischen und anorganischen Wasserinhaltstoffen schnell reagieren (LAMING et al. 1969, BAXTON und WILMARTH 1963, HOCHNADEL 1962):
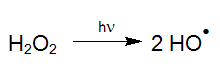
Die so generierten Hydroxylradikale (OH-Radikale) sind nicht nur mit dem geringsten Chemikalienaufwand hergestellt (Legrini et al. 1993) sondern auch mit dem wirtschaftlichsten Energieeinsatz (Bolton und Cater 1994). Daher ist dieses AOP-Verfahren (Advanced Oxidation Process) auch bei hohen Target-Konzentrationen besonders gut geeignet für eine effektive Schadstoffzerstörung in wässrigen Medien, wie hoch belastetem Abwasser, galvanischen Bädern bis hin zu hochreinem Prozesswasser, wobei im ppb-Bereich in der Regel Katalysatoren anstelle von H2O2 zum Einsatz kommen (siehe: UV-Deep-Clean).
Der Abbau von organischen Inhaltstoffen über OH-Radikale wird durch die Abstraktion von Wasserstoff eingeleitet (HABER und WILLSTÄTTER 1931):
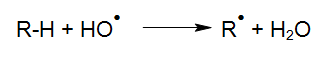
Bei Anwesenheit von Olefinen erfolgt eine elektrophile Addition der OH-Radikale:
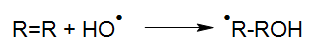
Diesen initiierenden Reaktionen folgen in der UV-Oxidation verschiedene Reaktionsmöglichkeiten der entstandenen Radikale. Bei Anwesenheit von Sauerstoff entsteht ein organisches Peroxylradikal:

Desweiteren können verschiedene Konkurrenzreaktionen eintreten:
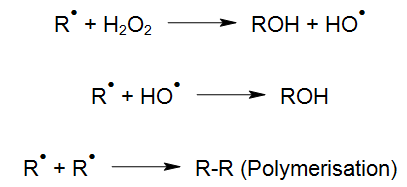
Dabei ist die Polymerisation in der Regel eine unerwünschte Reaktion in fast allen Anwendungen der UV-Oxidation, da die Polymerisationsprodukte zu einer Strahlerbelegung führen können. Deshalb muss bei der Reaktionsführung und der Konstruktion der Bestrahlungskammern streng darauf geachtet werden, dass eine Polymerisation unterbunden wird. Dazu dienen auch zusätzliche Prozesseinrichtungen, die die optimalen Reaktionsbedingungen für eine effiziente UV-Oxidation schaffen.
Auch das Peroxylradikal (RHO2• ) kann beispielsweise gemäß folgenden Gleichungen weiterreagieren:
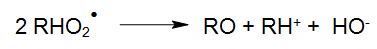
Die so entstandenen Aldehyde bzw. Ketone werden im weiteren Reaktionsverlauf zu Carbonsäuren oxidiert, welche einer thermischen oder photochemischen Decarboxylierung unterliegen (WEEKS und MATHESON 1955):

Typischer Verlauf wesentlicher Parameter bei der UV-Oxidation
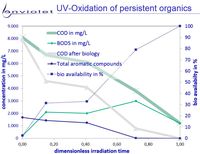
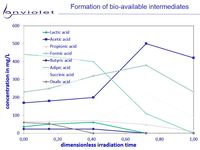
Bei der UV-Oxidation von schwer abbaubaren organischen Verbindungen nimmt die biologische Abbaubarkeit in fast allen Fällen sehr deutlich und rasch zu. Nur in sehr wenigen Fällen steigt die Bioverfügbarkeit nur geringfügig an.
Im Bild "Bildung von Abbauprodukten" ist erkennbar, dass als Abbauverbindungen fast ausschliesslich kleiner organische Karbonsäuren gebildet werden. Da diese Verbindungen ausnahmslos sehr gut biologisch Abbaubar sind, ist die starke Verbesserung der Bioverfügbarkeit durch die UV-Oxidation sehr gut erklärbar.
Typischer Farbverlauf eines konzentrierten Industrieabwassers während der Behandlung im Enviolet®-UV-Prozess.
Typischer Farbverlauf eines konzentrierten Industrieabwassers während der Behandlung im Enviolet®-UV-Prozess.








