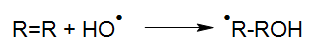uv reactors, photo-oxidation, advanced oxidation (aop), recycling & engineering
for industrial use
Chemie Van UV-Oxidatie en van geavanceerde oxidatie (advanced UV-oxidation)
Chemie van UV-Oxidatie
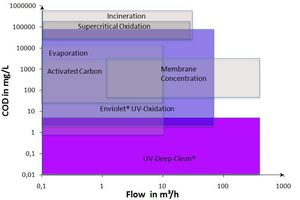
Enviolet is de specialist in UV-AOP bereik voor industriële toepassingen. Hierbij onderscheiden we twee verschillende procesfamilies: op basis van Foto-oxidatie en UV-oxidatie.
- Enviolet®: UV-oxidatie voor hogere concentraties in de homogene fase.
- UV Deep Clean: UV-oxidatie in de heterogene fase om zeer lage eindconcentraties te bereiken (UV/katalysator behandeling).
Grondbeginselen van UV-Oxidatie
De voorwaarde om een fotoreactie tot stand te brengen van een molecule R is de absorptie van licht door deze molecule (Calvert en Pitts, 1966). De hoeveelheid geabsorbeerd licht A(λ), wordt bepaald door de wet van Lambert-beer, waarbij I(0) de lichtintensiteit is voor de oplossing en I de lichtintensiteit nadat het licht de oplossing is gepasseerd. De absorptie is lineair afhankelijk van de concentratie C, de laagdikte d van de oplossing en de decadische extinctiecoëfficient ε(λ).
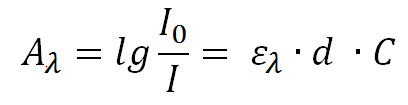
Bij absorptie van licht, met voldoende energie, ontstaat er uit de molecule R, een molecule R* met een verhoogde aangereikte energie, reactiever gemaakt door de toegevoegde foto-energie. In principe is de absorptie de vereiste voorwaarde voor elke fotoreactie. Dit betekend, allereerst, dat ook zeer donkere oplossingen (oplossingen met weinig lichtdoorlaatbaarheid) geschikt zijn om via fotochemie te behandelen, op voorwaarde dat de reactorbouw is aangepast.
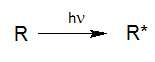
R* kan in deze toestand direct of via reactieve intermediairs naar zijn grondtoestand terugkeren of fysisch in fotoproducten verder reageren. Door aansluitende chemische processen ontstaan er in de waterige oplossing radicalen, radicaalionen, ionen of stabiele fragmenten, die door thermische processen verder kunnen reageren. In aanwezigheid van oxidatiemiddelen komen nog meer reacties tot stand.
Zo kan waterstofperoxide (H2O2) bv. Bij de juiste golflengte in hoog reactieve radicalen worden gefotoliseerd. Die radicalen reageren snel met organische en anorganische stoffen (LAMING et al. 1969, BAXTON en WILMARTH 1963, HOCHNADEL 1962)
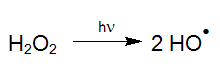
De op deze manier gegenereerde hydroxylradicalen (OH-Radicalen) zijn op zijn minst niet enkel voor de chemische aanwending ontstaan(Legrini et al. 1993), maar ook voor het rendabel inzetten van energie (Bolton en Cater 1994). Daarom is deze AOP behandeling bijzonder goed geschikt om hoge concentraties aan schadelijke stoffen af te breken in een waterig medium, zoals hoog belast afvalwater, galvanische baden, waarbij tot en met een hoog kwalitatief proceswater kan worden teruggegaan en waarbij in ppb bereik doorgaans gebruik gemaakt wordt van katalysatoren in plaats van waterstofperoxide. (zie: UV-Deep-Clean).
Het afbreken van organische stoffen door OH-Radicalen wordt door abstrahering van waterstof op gang gebracht (HABER en WILLSTÄTTER 1931):
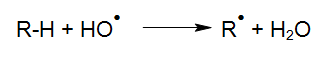
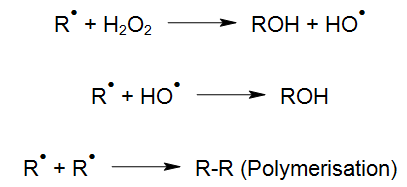
Deze initiërende reacties verlopen volgens verschillende reactiemogelijkheden naargelang de ontstane radicalen. Bij de aanwezigheid van zuurstof ontstaat er een organische peroxylradicaal:

Daarbij is polymerisatie doorgaans een ongewenste reactie in bijna alle toepassingen van UV-oxidatie, omdat die polymerisatieproducten zich meestal op de lampen afzetten. Derhalve moet, bij het sturen van de reactie en bij de reactorkamerconstructie, er erg op gelet worden dat de polymerisatie verhinderd wordt. Hierbij wordt ook de aanvullende procesinrichting gerekend, die de ideale reactiecondities voor een efficiënte oxidatie moet verschaffen. Ook het peroxylradicaal (RHO2• ) kan bv. volgens volgende reactievergelijkingen verder reageren:
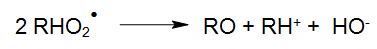
De zo gevormde aldehyden (bv. Ketonen) worden in een verdere reactieverloop tot koolzuur geoxideerd, die onderhevig zijn aan thermische of een fotochemische decarbolisering (WEEKS en MATHESON 1955):

Typisch verloop van afbraakproducten tijdens UV-oxidatie
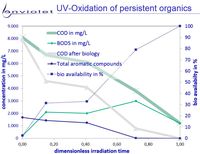
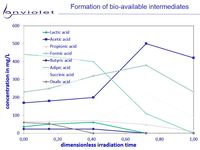
Tijdens de UV-oxidatie van moeilijk afbreekbare organische verbindingen, neemt de biologische afbreekbaarheid in bijna alle gevallen zeer duidelijk en vlug toe. Sporadisch gaat de bio-toegankelijkheid maar traag omhoog.
In de grafieken is duidelijk te zien, dat de afbraakproducten van de UV-oxidatie kleine organische carbonzuren zijn, die gemakkelijk biologisch kunnen afgebroken worden. Dit laatste verklaard hoe UV-oxidatie de biologische toegankelijkheid sterk verbeterd.
Typisch kleurverloop van een geconcentreerd industrieel afvalwater tijdens het Enviolet®-UV-Proces
Typisch kleurenverloop van een geconcentreerd industrieel afvalwater tijdens het Enviolet®-UV-Proces