UV-Oxidation
Foto-Oxidation
Zyanid-Abbau
Einordnung von Cyaniden
Cyanid, das in Wasser oder Abwasser vorkommen kann, wird in drei Klassen unterteilt:
1.) Freies Cyanid (umfasst CN-)
2.) Leicht Freisetzbares Cyanid
(umfasst CN- sowie schwache bis mittelstarke Komplexe wie Kupfercyanide, Nickelcyanide und Silbercyanide)
3.) Gesamt Cyanid (umfasst alle vorliegenden Cyanide inklusive sehr starker Komplexe wie Cyanoferrate und Kobaltcyanide)
Diese Einteilung entspricht den entsprechenden Analysenparametern, die durch DIN Methoden definiert sind. Diese Messgrößen sind sogenannte Methoden-abhängige Parameter, was dadurch begründet ist, dass eine eindeutige Eingruppierung des Cyanidgehaltes eines Wassers in der Regel nicht möglich ist, da selten eine Spezies alleine vorliegt, sondern eine Mischung von Cyanokomplexen verschiedener Metalle.
Cyanid-Oxidation mit Chlorbleichlauge
Die Behandlung von cyanidischem Abwasser mit Chlor, d.h. in der Regel mit Chlorbleichlauge (Natriumhypochlorit-Lösung) stellt das traditionelle Verfahren zur Entgiftung dar.
Lange Zeit war dieses Verfahren Stand der Technik, da es bei relativ geringen Investitionskosten meist zum gewünschten Behandlungsergebnis führte.
Zunehmend wird die Entgiftung mit Hypochlorit aus folgenden Gründen infrage gestellt oder muss in Betrieben ersetzt werden:
1.) Durch die Reaktion von Chlor mit organischen Inhaltstoffen wie z.B. Tensiden und Komplexbildnern entstehen chlorierte Substanzen, die als AOX erfasst werden und häufig zur Überschreitung dieses Grenzwertes führen.
2.) Es entstehen neben AOX auch weitere chlorierte problematische Substanzen: Das Tränengas Chlorcyan in der ersten Reaktionsphase und gegen Ende der Behandlung die toxischen Chloramine.
3.) Je nach Zusammensetzung der vorliegenden Metalle gestaltet sich eine erfolgreiche Entgiftung des Abwassers als langwierig oder auch unmöglich.
4.) Nach einer Behandlung mit Chlorbleichlauge liegen meist noch andere Komplexbildner vor, die den Einsatz von großen Mengen an sulfidischem Fällungsmittel erforderlich machen.
5.) Der Verbrauch von Chlorbleichlauge liegt in der Praxis bei dem 4-fachen des stöchiometrischen Verbrauchs, da das Hypochlorit mit dem gebildeten Ammoniak zu Trichloramin weiterreagiert.
Trichloramin ist im Abwasser nicht zulässig.
Landesämter, wie das baden-württembergische Ministerium für Umwelt, Klima und Energiewirtschaft, empfehlen mittlerweile die Cyanid-Behandlung durch das UV/H2O2 Verfahren, da dies das umweltfreundlichere Verfahren darstellt.
UV/H2O2 Behandlung von Cyaniden
Der fotochemische Abbau von Cyaniden (UV-Oxidation) wird von einer Vielzahl von Reaktionen herbeigeführt, die je nach Zusammensetzung der Wasserinhaltstoffe und der oben genannten Cyanidkomplexe unterschiedliche Gewichtungen haben. Zudem sind die exakten Mechanismen relativ selten untersucht worden und es liegen in der Literatur teilweise widersprüchliche Angaben zu den möglichen Reaktionswegen der UV-Oxidation von Cyaniden vor.
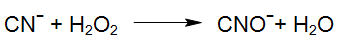
Schon Wasserstoffperoxid allein, d.h. ohne UV-Strahlung, führt bei geeigneten Bedingungen zu einer Oxidation des freien und einem Teil des leicht freisetzbaren Cyanides, wobei je nach Stabilität der Komplexe sehr lange Reaktionszeiten erforderlich sind.
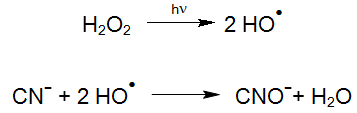
Das aus der photolytischen Spaltung von H2O2 (H2O2/UV) gewonnenen Hydroxylradikal reagiert ebenso mit Cyanid:
Insbesondere bei der Oxidation von stabileren Metall-Cyano Verbindungen spielt die Anregung des Metall-Cyano Komplexes durch die UV-Strahlung (UV-Oxidation / UV-H2O2-Oxidation) eine bedeutende Rolle, da dieser im angeregten Zustand schnell mit Wasserstoffperoxid reagieren kann:
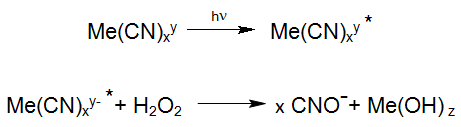
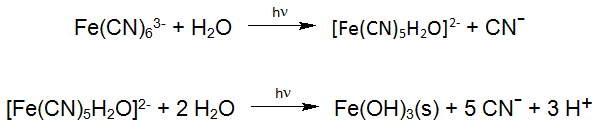
Als bekannte fotochemische Reaktion ist der Abbau der stabilen Hexacyanoferraten zu nennen, die in der solaren Fotochemie von Oberflächenwässern häufig untersucht werden. Diese Reaktionen finden auch beim industriellen Einsatz des enviolet® Verfahrens bei der UV-H2O2-Behandlung von Hexacyanoferrat-haltigem Abwasser statt, mit dem Ziel das Gesamt-Cyanid abzubauen (z.B. Verichrome (U.K.): bis zu 1500 mg/L auf < 1 mg/L).
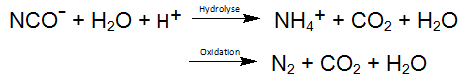
Entsprechend obiger Gleichungen wird das so freigesetzte Cyanid zum Cyanat oxidiert. Eine entsprechende Reaktion findet sogar bei der Photolyse der Kobaltcyanid-Komplexe statt, der den stabilsten MeCN –Komplex darstellt. Das aus den oben beschriebenen Reaktionen hervorgehende Oxidationsprodukt Cyanat reagiert leicht durch Hydrolyse zu Kohlendioxid und Ammonium, wobei auch die Oxidation des Cyanats zu Stickstoff und Kohlendioxid als Nebenreaktion möglich ist.
UV/H2O2 Behandlung von organischen Cyaniden
Neben der UV-Oxidation von anorganischem Cyanid, können auch organische Cyanide, d.h. Nitrile durch das Enviolet® Verfahren oxidiert werden, wobei hier die Reaktionen, die unter CSB/TOC Abbau beschrieben sind, zum Tragen kommen. Nitrile können unter bestimmten Bedingungen durch Hydrolyse Cyanid freisetzen wodurch eine entsprechende Entgiftung des Wassers erforderlich wird.
Cyanidoxidation bei realem Abwasser

In der Abwasser- oder Grundwasseraufbereitung liegen normalerweise keine reinen Belastungen durch Cyanide vor, da deren industrielle Anwendung meist auch organische Inhaltstoffe wie Tenside oder organische Komplexbildner erfordert. Zudem liegt nur selten ein reines Abwasser aus einem Produktionsstrang vor, oft ist dieses mit anderen Abwasserarten, teils aus diffusen Quellen, vermischt.
Bei der Behandlung dieser realen Abwässer stehen die für den Cyanidabbau genannten Reaktionen in Konkurrenz mit Reaktionen der organischen Inhaltsstoffe. Um die ungewollten Reaktionen zu minimieren, werden die Reaktions-Bedingungen und –Parameter der UV-Oxidation an die im Werk übliche Abwasserzusammensetzung angepasst. Teilweise sind „Nebenreaktionen“ aber auch erwünscht und werden gefördert, wenn diese beispielweise zum Abbau organischer Komplexbildner führen. Der Einsatz von teurem Organosulfid für die Fällung der Schwermetalle kann dann vermindert werden oder meist sogar völlig entfallen.
Diese Optimierungsmöglichkeiten gewährleisten ein wirtschaftliches Verfahren mit minimalen Investitions- und Betriebskosten auch bzw. gerade bei komplexer Zusammensetzung des Abwassers. So ist z.B. auch die Behandlung von Abwasser, welches sowohl Cyanid als auch EDTA enthält, problemlos möglich (Industriebeispiel: Miba Gleitlager (Österreich); DOW (Schweiz)).
Zyanid-Oxidation in Grundwasser
Der Abbau von Cyaniden im Grundwasser mittels UV-Oxidation ist meist ohne weiteres möglich!
Beispiel: Behandlung von Grundwasser
Ausgangskonzentrationen der betrachteten Brunnen:
Brunnen 1: T-CN (Cyanid, gesamt): 2,9 mg/L
Brunnen 2: T-CN (Cyanid, gesamt): 0,18 mg/L
Zielsetzung des UV/H2O2 Prozesses:
Erreichen des Zielwertes von <50 µg/L durch die UV-Oxidation
Zyanid-Abbau in Industrieabwasser
In Industrieabwässern ist die Zyanid-Oxidation meist eine Vorstufe vor der Metallfällung.
Beispiel: Behandlung von Cyanid- und EDTA-haltigem Industrieabwasser
Typische Abwasserwerte:
- Cyanid, leicht freisetzbar: 550 mg/L
- EDTA: 230 mg/L
- TOC (total organic carbon): 1320 mg/L
Zielsetzung des UV/H2O2 Prozesses:
- Einhaltung des Grenzwertes von 0,2 mg/L leicht freisetzbares Cyanid.
- Zerstörung von EDTA und weiterer organischer Komplexbildner durch die UV-Oxidation damit die nachfolgende Metallfällung zur Einhaltung der Metallgrenzwerte führt
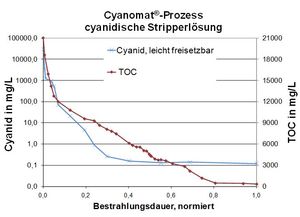
Zyanid-Oxidation in Stripperlösung
Zuverlässiger Abbau von Cyanid-Komplexen auch in stark gefärbten Lösungen!
Viele Stripperlösungen in der Oberflächentechnik enthalten Cyanid zur Entfernung der unerwünschten Metallschicht und ein Reduktionsmittel zum Schutz der darunterliegenden Schicht.
Diese Stripper sind in der Entsorgung sehr teuer und können in unserem Cyanomat-Prozess kostengünstig behandelt werden.
Beispiel: Behandlung von Cyanid-haltigen Stripperlösungen
Typische Abwasserwerte:
- Cyanid, gesamt: 50.000 mg/L
- TOC (total organic carbon): 21.000 mg/L
Zielsetzung des UV/H2O2 Prozesses:
- Einhaltung des Grenzwertes von 0,2 mg/L leicht freisetzbares Cyanid.
- Zerstörung von weiteren organischen Inhaltstoffen (z.B. Nitrobenzolsulfonat) durch die UV-Oxidation damit die nachfolgende Metallfällung zur Einhaltung der Metallgrenzwerte führt.