uv reactors, photo-oxidation, advanced oxidation (aop), recycling & engineering
for industrial use
Degradazione Cyanide
Classificazione dei cianuri
Cianuro, che può verificarsi in acqua o acqua di scarico, è suddiviso in 3 classi:
1.) Cianuro libero (comprende CN-)
2.) Cianuro dissociabile facilmente (comprende CN- e deboli a moderatamente forti complessi quali cianuri di rame, di nichel e d’argento)
3.) Cianuro complessivo (questo include tutti i cianuri compresi i complessi cianuro molto forti come cianuro di ferro e cobaldo)
Questa divisione corrisponde ai rispettivi parametri di analisi che sono definiti dai metodi DIN. Queste misure sono chiamate parametri metodo-dipendenti, che si giustifica dal fatto, che un chiaro raggruppamento del contenuto di cianuro dell'acqua non è generalmente possibile, che raramente vi è una sola specie ma una miscela di ciano complessi di vari metalli
Ossidazione cianuro con candeggina clorata
Il trattamento delle acque reflue contenenti del cianuro con cloro, che di solito avviene con candeggina clorata (ipoclorito di sodio) rappresenta il metodo tradizionale per la disintossicazione. Per lungo tempo questo metodo era stato della tecnica, poiché a investimenti relativamente contenuti solitamente portava al risultato desiderato.
Sempre più spesso, la disintossicazione con ipoclorito è messa in discussione per i seguenti motivi o deve essere sostituita nelle aziende:
1.) Dalla reazione del cloro con sostanze organiche come Tensioattivi e agenti complessanti sono prodotte delle sostanze clorurate, che vengono rilevate come AOX e spesso portano a superare questo limite..
2.) Oltre l‘AOX si formano anche delle sostanze clorurate più problematiche: Il gas lacrimogeno cloruro di cianogeno nel primo stadio di reazione e al termine del trattamento le clorammine tossiche.
3.) A seconda della composizione dei metalli presenti, una disintossicazione delle acque reflue riuscita si presenta complicata o perfino impossibile.
4.) Dopo il trattamento con candeggina clorata di solito ci sono altri agenti complessanti, che possono richiedere l'uso di grandi quantità di agenti precipitanti al solfuro.
5.) Il consumo di candeggina clorata in pratica è 4 volte del consumo stechiometrico, poiché l'ipoclorito reagisce ulteriormente con l'ammoniaca formata per trichloramine. Trichloramine non è ammesso nelle acque reflue..
Uffici statali, come ad esempio il Baden-Württemberg Ministero dell'Ambiente, Clima ed Energia, ora consigliano il trattamento cianuro con il processo UV/H2O2, in quanto questo è il metodo più ecologico.
Trattamento di cianuri UV/H2O2
La degradazione fotochimica di cianuri (ossidazione UV) è causata da una varietà di reazioni, le quali secondo la composizione del contenuto di acqua e i suddetti complessi di cianuri hanno una valutazione diversa. Inoltre, i meccanismi esatti sono stati studiati abbastanza raramente e vi sono nella letteratura alcune informazioni contrastanti sui possibili percorsi di reazione di ossidazione UV dei cianuri.
Anche solo perossido d’idrogeno, cioè senza radiazione UV, in adatte condizioni porta all’ossidazione del cianuro libero o una parte prontamente rilasciabile, e in funzione della stabilità dei complessi occorrono dei tempi di reazione molto lunghi.
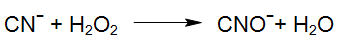
Il radicale idrossile prodotto dalla scissione fotolitica di H2O2 (H2O2/UV) reagisce altresì con il cianuro:
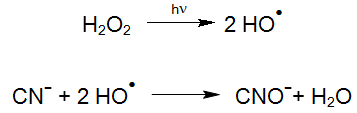
In particolare, nell'ossidazione dei composti metallo-ciano più stabili l’incentivo del complesso metallo-ciano tramite radiazione ultravioletta (ossidazione UV / ossidazione UV H2O2) ha una funzione importante, perché può rapidamente reagire con il perossido d’idrogeno in stato stimolato.
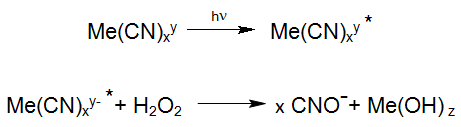
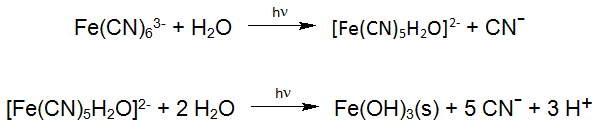
Una reazione fotochimica ben nota è la degradazione degli esacianoferrati stabili, che sono spesso studiati nella fotochimica solare delle acque superficiali. Queste reazioni hanno luogo anche con l‘applicazione industriale del procedimento®Enviolet nel trattamento UV-H2O2 di acque reflue, contenenti esacianoferrato, con l'obiettivo di degradare il cianuro totale (Eg Verichrome (UK): fino a 1500 mg / L, <1 mg / L).
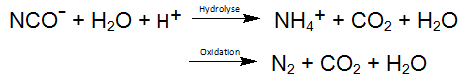
Secondo le precedenti equazioni il cianuro così liberato è ossidato a cianato. Una reazione simile avviene anche durante la fotolisi dei complessi cobalto cianuro, che rappresenta il complesso più stabile di MeCN. Il prodotto d’ossidazione derivante dalle reazioni succitate, cianato, reagisce facilmente per idrolisi ad anidride carbonica e ammonio, in cui l'ossidazione del cianato è possibile ad azoto e anidride carbonica come reazione collaterale:
Trattamento UV/H2O2 dei cianuri organici
Oltre all‘ossidazione UV di cianuri inorganici, anche cianuri organici, vale a dire nitriti possono essere ossidati con il procedimento ®Enviolet, nel qual caso le reazioni che sono descritte sotto COD / TOC degradazione, entrano in azione. A determinate condizioni, nitriti per idrolisi possono rilasciare del cianuro, quindi una disintossicazione adeguata dell'acqua è necessaria.
Ossidazione cianuro nelle acque reflue reali

Nel trattamento delle acque reflue o sotterranee di solito non sussistono dei carichi puri di cianuro, perché la loro applicazione industriale richiede solitamente ingredienti organici, quali tensioattivi o complessanti organici. Inoltre si trova raramente dell’acqua reflua pura da una linea di produzione, questa è spesso mescolata con altri tipi di acque reflue in parte da fonti diffuse.
Nel trattamento di queste acque reflue reali le reazioni citate per la degradazione di cianuro sono in concorrenza con le reazioni d’ingredienti biologici. Per minimizzare le reazioni indesiderate, le condizioni di reazione e parametri dell’ossidazione UV sono adattate alla consueta composizione di reflui fabbrica. Parzialmente le “reazioni collaterali” sono anche auspicabili e sono promosse, per esempio, se questo comporta la degradazione di agenti complessanti organici. L'uso di costosi organosulfidi per la scissione dei metalli pesanti può essere ridotto o addirittura completamente eliminato.
Queste possibilità di ottimizzazione assicurano un processo economico con i minimi costi d’investimento e di esercizio, anche risp. Addirittura con una composizione complessa delle acque reflue. Così, per esempio anche il trattamento di acque reflue contenenti sia cianuro e EDTA, è possibile (Esempio industriale: Miba Gleitlager (Austria); DOW (Svizzera))
L'ossidazione cianuro nelle acque sotterranee
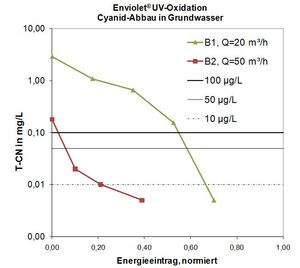
La degradazione del cianuro nelle acque sotterranee mediante l'ossidazione UV di solito è facilmente possibile.
Esempio 1:
Concentrazioni attuali del rispettivo pozzo:
Pozzo 1: T-CN (cianuro, totale): 2,9 mg/L
Pozzo 1: T-CN (cianuro, totale): 0,18 mg/L
Obiettivo del processo UV/H2O2:
Raggiungimento del valore obiettivo di 50 g / L tramite ossidazione UV
Degrado cianuro negli scarichi industriali
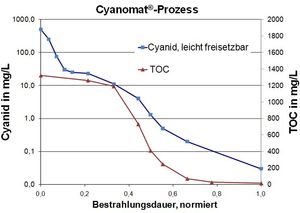
Negli scarichi industriali l'ossidazione cianuro di solito è un primo grado della scissione metalli.
Esempio: Reflui industriali contenenti Cyanide ed EDTA.
Valori tipici degli scarichi:
Cyanide, facilmente liberabile: 550 mg/L
EDTA: 230 mg/L
TOC (total organic carbon): 1320 mg/L
Obiettivo del processo UV/H2O2:
Adempimento del valore obiettivo di 0,2 mg/L Cyanide, facilmente liberabile.
Distruzione di EDTA e di altri agenti complessanti organici mediante ossidazione UV, in modo che la successiva eliminazione di metallo conduce al rispetto dei valori limite di metallo.
Ossidazione cianuro in soluzione estrattore
Molte soluzioni estrattore nella tecnologia delle superfici contengono cianuro per l’eliminazione di uno strato di metallo non desiderato e un agente riducente per la protezione dello strato sottostante. Questi estrattori sono molto costosi da smaltire e possono essere trattati nel nostro Processo Cyanomat a basso costo.
Esempio: soluzione estrattire contenente cianuro
Valori tipici degli effluenti:
Cianuro, totale: 50.000 mg/L
TOC (total organic carbon): 21.000 mg/L
Obiettivo del procedimento UV/H2O2:
Rispetto del valore limite di 0,2 mg/L cianuro facilmente rilasciabile.
Distruzione di altri ingredienti biologici (eg. nitrobenzenesulfonate) tramite l‘ossidazione UV, in modo che la successiva scissione dei metalli conduca al rispetto del limite di metalli.